隨著癌症治療技術的進步,患者的存活率顯著提升,但隨之而來的副作用卻成為新的挑戰。其中,「化療引起的末梢神經病變」(Chemotherapy-induced peripheral neuropathy, CIPN)是許多化療病患面臨嚴重影響生活品質的問題之一。
CIPN的普遍性與治療困境
CIPN 主要由常見的化療藥物如紫杉醇類(taxanes)、鉑類(platinum agents)、長春花生物鹼(vinca alkaloids)以及某些標靶藥物(如蛋白酶體抑制劑)所引起。這些藥物在殺死癌細胞的同時,也損害了末梢神經的結構與功能 [1, 2]。患者常描述手腳末端出現對稱性的麻木、刺痛、燒灼感,甚至產生對溫度或觸覺的異常敏感,嚴重時會影響精細動作(如扣鈕扣)及行走平衡 [4]。
根據 Seretny 的系統性文獻回顧與統合分析(Systematic review and meta-analysis)指出,CIPN 的發生率相當驚人:在化療結束後第一個月,發生率高達 68.1%;即便在六個月後,仍有約 30% 的患者持續受症狀困擾 [3]。
然而,面對如此高發的併發症,現代醫學在藥物治療上卻面臨巨大瓶頸。根據美國臨床腫瘤醫學會(ASCO)的臨床指引,目前「沒有」任何藥物被推薦用於「預防」CIPN 的發生。在「治療」已發生的疼痛方面,唯一獲得中度推薦證據等級的藥物僅有抗憂鬱劑Duloxetine (常見商品名”千憂解”) [5, 6]。其他常被使用的藥物如加Gabapentin (常見商品名” 鎮頑癲”),在指引中並未被推薦,且這些口服藥物常伴隨嗜睡、頭暈等副作用,限制了臨床使用 [2, 5]。因此,尋求安全、有效的非藥物治療策略變得至關重要 [4]。
非藥物治療新曙光:結合傳統智慧與現代科技
鑑於藥物選擇有限,臨床研究逐漸將目光轉向非藥物介入。其中,源自傳統醫學的針灸以及現代物理治療中的神經電刺激療法,因其安全性高且副作用極少的特性,成為備受矚目的輔助治療選項。
1. 針灸療法:源自傳統的實證治療
針灸作為傳統中醫學的重要組成部分,近年來在 CIPN 的治療上獲得了越來越多的科學實證支持。
- 臨床證據與效益: 根據 Li 等人於 2020 年發表的一項系統性文獻回顧與統合分析,針灸被證實能有效緩解 CIPN 患者的臨床症狀。分析結果顯示,與對照組相比,接受針灸治療的患者在疼痛強度和麻木感方面均有顯著改善。更重要的是,客觀的神經傳導檢查也顯示,針灸有助於改善感覺神經和運動神經的傳導速度 [7]。
- 作用機制與安全性: 針灸被認為透過刺激特定的穴位,調節體內的能量流動(氣),並促使神經系統釋放內源性鴉片類物質(如腦內啡)和其他神經傳導物質,從而達到止痛和修復神經的作用。該研究也強調,針灸治療 CIPN 的安全性相當高,極少出現嚴重的不良反應,使其成為一個值得考慮的輔助治療選擇 [7]。
2. 經皮神經電刺激器 (TENS):居家疼痛管理利器
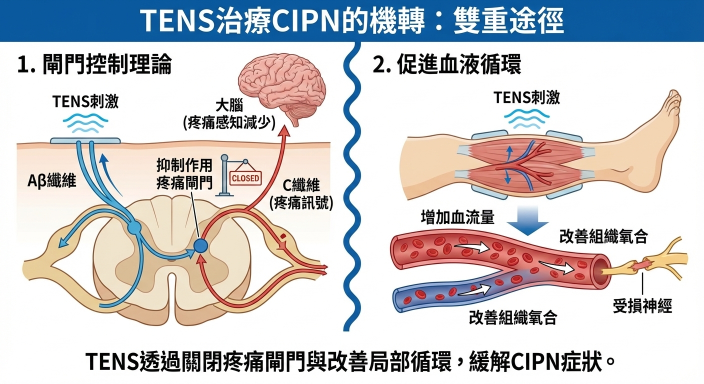
- 作用機制: TENS 的核心機制基於「門控理論」(Gate Control Theory)。它藉由刺激較粗的感覺神經纖維(Aβ纖維),搶先佔據脊髓中傳遞訊號的「閘門」,從而阻斷或減少細神經纖維(C纖維和Aδ纖維)傳入大腦的疼痛訊號。此外,低頻率的 TENS 刺激也被認為能促進人體釋放內源性鴉片類物質,達到自然止痛的效果 [4]。
- 臨床應用優勢: 對於 CIPN 患者,TENS 的最大優勢在於它是一種便宜、安全,且患者經過指導後可在家中自行操作的設備。研究顯示,TENS 有助於減輕疼痛強度、減少異常感覺(如針刺感),並改善患者的日常生活活動能力 [4]。
康復特波電刺激器的特色與CIPN的可能應用
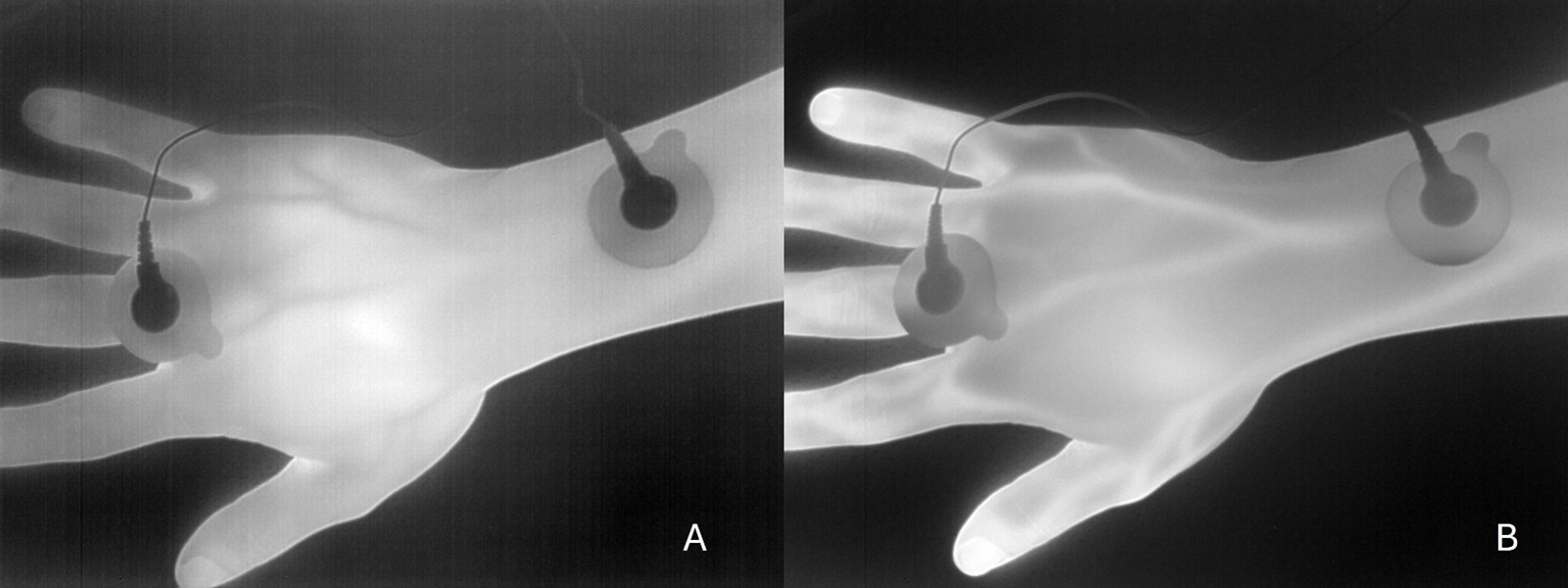
康復特波電刺激器獲得的適應症中,就包含促進局部血液循環及治療末稍神經麻痺的功效。除了運用Gate therapy來止痛外,促進局部血液循環也可以避免神經細胞的壞死及幫助神經的再生 (如圖一)。此外,因為康復特波電刺激器特有的”單向波”設計,應用於穴道上的電刺激可模擬中醫經絡順逆的方向性,達到經絡治療效果。由高精度熱顯像儀顯示,使用康復特波,只要輕輕電,不引起肌肉抽動下,即可可快速促進末梢局部血液循環 (如圖二)。
<圖一>
<圖二>
A. 治療前 B. 治療約2分鐘,可以看到末梢血管顯像亮起來(代表溫度上升); 治療區域雖然只有在第三指,但是五隻手指的血管都一起變明顯。
結語
在化療引起的末梢神經病變缺乏特效藥的現狀下,非藥物治療提供了重要的輔助角色。患者們可去尋求針灸療法,來改善神經傳導和緩解相關麻木的症狀;而居家電刺激器的使用,則提供了一種便利的居家疼痛管理手段。建議有需求的患者在尋求電刺激治療來緩解CIPN時,可諮詢專業醫師或物理治療師,以制定最適合個人的治療計畫。
參考文獻 :
[1] Majithia, N., Loprinzi, C. L., & Smith, T. J. (2016). New Practical Approaches to Chemotherapy-Induced Neuropathic Pain: Prevention, Assessment, and Treatment. Oncology. 30(11): 1020–1029.
[2] Velasco, R., & Bruna, J. (2021). Taxane-Induced Peripheral Neurotoxicity. Neurotherapeutics. 18: 1436–1449.
[3] Seretny, M., Currie, G. L., Sena, E. S., Ramnarine, S., Grant, R., MacLeod, M. R., Colvin, L. A., & Fallon, M. (2014). Incidence, prevalence, and predictors of chemotherapy-induced peripheral neuropathy: A systematic review and meta-analysis. Pain, 155(12): 2461–2470.
[4] Wasilewski, D., & Zychowska, M. (2022). Non-Pharmacological Treatment of Chemotherapy-Induced Peripheral Neuropathy (CIPN)—A Current Overview of Methods. Medicina, 58(3): 284.
[5] Hershman, D. L., Lacouture, M. E., Ion, S., Loprinzi, C. L., Scavone, J. L., Novotny, P. J., ... & American Society of Clinical Oncology. (2014). Prevention and management of chemotherapy-induced peripheral neuropathy in survivors of adult cancers: American Society of Clinical Oncology clinical practice guideline. Journal of Clinical Oncology. 32(18): 1941-1967.
[6] Smith, T. J., & Loprinzi, C. L. (2020). Prevention and management of chemotherapy-induced peripheral neuropathy in survivors of adult cancers: ASCO guideline update. CA: A Cancer Journal for Clinicians. 70(6): 425-425.
[7] Li, K., Giustini, D., & Seely, D. (2020). Acupuncture for chemotherapy-induced peripheral neuropathy: A systematic review and meta-analysis. Medicine. 99(20): e19837.
